
Новый штамм циповируса DsCPV-1, выделенный из гусениц сибирского шелкопряда (Dendrolimus sibiricus), рассматривается как перспективный биологический инсектицид против насекомых-вредителей. Для массового производства этого вируса был предложен кандидат продуцент — табачный бражник (Manduca sexta), насекомое с коротким жизненным циклом и низкой стоимостью разведения. Исследования подтвердили активную репликацию вируса в M. sexta, однако выявили необычную особенность: в клетках кишечника накапливались преимущественно «голые» вирионы без защитных белковых оболочек — полиэдров. В то время как в основном хозяине, сибирском шелкопряде, полиэдры образуются обильно, обеспечивая устойчивость вируса во внешней среде и горизонтальную передачу инфекции (Subbotina et al., 2025, Journal of economic entomology).
Сохранит ли вирус, выработанный личинками M. sexta, эффективность против целевых насекомых-вредителей? Эксперименты дали обнадёживающий ответ для борьбы с сибирским шелкопрядом: новый штамм вызывал до 73% смертности, а образование полиэдров в заражённых личинках полностью восстанавливалось. Что критически важно для поддержания цепи заражения в популяции. Однако при испытаниях на непарном шелкопряде (Lymantria dispar) ни пассаж, полученный от основного хозяина, ни пассаж, полученный от альтернативного хозяина, не вызывали значимой гибели личинок средних возрастов, несмотря на подтверждённую репликацию вируса (Subbotina et al., 2025, Insects). Вероятно, у этих гусениц развивается толерантность — способность переносить инфекцию без гибели. Кроме того, в их организме полиэдры формировались в значительно меньших количествах. Таким образом, M. sexta остаётся перспективным продуцентом для препарата на основе DsCPV-1 против сибирского шелкопряда, но для борьбы с другими вредителями потребуются дополнительные исследования и оптимизация состава биоинсектицида.
Рисунок — Микроскопия вирионов и полиэдров вируса DsCPV-1. Верхний ряд: электронная микроскопия вирионов в клетках кишечника табачного бражника (M. sexta). Нижний ряд: световая микроскопия полиэдров DsCPV-1 (слева) и их ультраструктура с характерными вирионами внутри (справа). Синие стрелки указывают на ключевые элементы: «голые» вирионы (верхний ряд) и кристаллические полиэдры (нижний ряд).
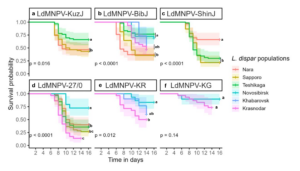
В журнале Scientific Reports были опубликованы результаты исследований, где авторы сравнили эффективность разных изолятов бакуловируса непарного шелкопряда LdMNPV и связали наблюдаемые различия с особенностями геномов вируса (Akhanaev et al., 2025, Scientific Reports). В биотестах использовали несколько популяций Lymantria dispar из России и Японии (включая разные подвиды), а также близкий вид L. umbrosa (Хоккайдо). Заражение проводили перорально методом спаивания вирусной суспензии в фиксированных дозах; для российских популяций применяли дозы 5–5000 полиэдров на личинку, для японских популяций использовали одну дозу 50 пол/личинку, смертность учитывали 16 дней. Было показано, что эффективность вируса ядерного полиэдроза не сводится к простому правилу «местный изолят эффективнее на местной популяции». Так, сибирский изолят LdMNPV-27/0 оказался более эффективным против краснодарской популяции, по сравнению с локальным изолятом LdMNPV-KR, а изолят LdMNPV-KG (Киргизстан) почти не действовал на личинок из Новосибирска, но снижал выживаемость у краснодарских личинок. В целом новосибирская популяция демонстрировала повышенную выживаемость. Для трёх новых изолятов (KR, KG, BibJ) выполнено полногеномное секвенирование: геномы различались по размеру (примерно 153,8–164,5 тыс. п.н.) и, в частности, по числу генов семейства bro; у изолята BibJ выявлено отсутствие гена vef-1, однако вопреки ожиданиям, это не гарантировало низкую вирулентность.
Практический вывод для разработки биопрепаратов: важны свойства конкретного штамма, поэтому нужен отбор «лучшего» изолята по биотестам, а не ставка только на взаимодействие географий популяций хозяина и вируса.
Рисунок 2. Динамика выживания популяций непарного шелкопряда при пероральном заражении различными изолятами LdMNPV. Кривые обозначены разными буквами при наличии статистически значимых различий (log-rank тест с поправкой Holm, p < 0,05).
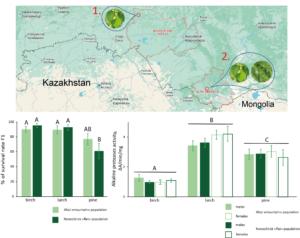
Была исследована адаптивная способность азиатских популяций непарного шелкопряда (Lymantria dispar) к питанию хвойными породами (Arzhanova et al., 2026, Scientific Reports). Данная работа была проедена в контексте потенциального изменения климата и связанного с этим расширении ареала вредителя (Ponomarev et al., 2023). Сравнивались две популяции: новосибирская (питающаяся преимущественно берёзой Betula pendula) и алтайская (использующая как берёзу, так и лиственницу Larix sibirica). Личинок выращивали на трёх видах кормовых растений: берёзе (контроль), лиственнице и сосне обыкновенной (Pinus sylvestris). Выживаемость личинок обеих популяций при питании на лиственнице не отличается от берёзы, тогда как у новосибирской популяции снижается при питании на сосне. Алтайская популяция демонстрирует одинаковую выживаемость на всех трёх кормовых растениях, что сохраняется и во втором поколении. Питание сосной приводит к снижению массы куколок и удлинению личиночной стадии у обеих популяций. Количество отложенных яиц уменьшается при питании на сосне, но не на лиственнице. При этом, отрождение насекомых не зависит от кормового растения.
Физиологические исследования выявили повышение активности щелочных протеаз в средней кишке при питании хвойными по сравнению с берёзой, а также накопление малонового диальдегида (маркера окислительного стресса) на лиственнице. Активность эстераз увеличивается только у самцов алтайской популяции при питании сосной.
Таким образом, непарный шелкопряд обладает достаточной физиологической пластичностью для освоения хвойных хозяев, особенно при наличии «промежуточного» хозяина – лиственницы. Это повышает риск его успешного северного расширения и потенциального негативного воздействия на бореальные леса.
Рисунок — Сравнение физиологических параметров двух популяций непарного шелкопряда при выращивании на разных видах кормовых растений.
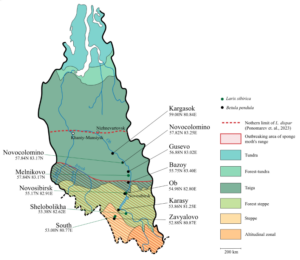
Другое исследование для изучения потенциальной адаптации непарного шелкопряда к серверным популяциям растений-хозяев при его экспансии на север было проведено в Западной Сибири (Subbotina et al., 2025, Forest Ecology and Management). В исследовании изучалась роль химических защитных соединений берёзы повислой (Betula pendula) и лиственницы сибирской (Larix sibirica), ассоциированная с широтой произрастания растений, в потенциальном сдерживании северной экспансии непарного шелкопряда (Lymantria dispar) — одного из наиболее опасных лесных фитофагов Евразии.
Исследование проводилось в Западной Сибири, где в пределах различных природных зон (см. рис.) были собраны листья березы и хвоя лиственницы. Отбор листьев осуществлялся ранней весной — в период активного питания гусениц и их повышенной чувствительности к химическим защитным соединениям растений. У лиственницы выявлена чёткая широтная закономерность: к северу содержание двух соединений с доказанным антфидантным действием — дегидроабиетиновой кислоты и нонакозан-10-ола — значительно снижалось. Одновременно возрастала концентрация жирных кислот, включая α-линоленовую, играющую ключевую роль в иммунных реакциях растений. У берёзы повислой картина оказалась сложнее: концентрация тритерпеноидов, обладающих токсичностью для гусениц непарного шелкопряда, изменялась нелинейно в зависимости от широты. Важно, что северные популяции берёзы не демонстрировали повышенного уровня защитных метаболитов по сравнению с южными. Полученные данные свидетельствуют о слабости химического барьера растений на пути северного распространения непарного шелкопряда. Снижение концентрации антфидантных соединений у лиственницы на севере и отсутствие усиления химической защиты у берёзы создают благоприятные условия для освоения новых территорий вредителем в условиях продолжающегося потепления. Эти результаты подчёркивают критическую важность превентивного контроля вспышек численности непарного шелкопряда на северной границе его ареала для сохранения устойчивости сибирской тайги.
Рисунок — Исследуемая территория и точки сбора образцов для фитохимического анализа.
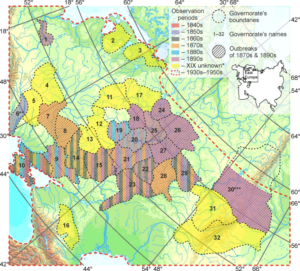
Поскольку недавно усилиями нашей лаборатории, совместно с коллегами энтомологами из Екатеринбурга и Квебека (Канада) было показана экспансия непарного шелкопряда на север в центральной части его ареала (Ponomarev et al., 2023), мы поставили задачу актуализировать северную границу ареала вида в западной части ареала. Таким образом мы поревели мониторинг Северо-Запада России на заселенность непарным шелкопрядом, а заодно осуществили ретроспективный анализ заселённости данным видом европейской части России за последние 200 лет (Selikhovkin et al., 2025, Insects). Нами было показано, что в разных участках ареала картина существенно отличается. Если в Западной Сибири непарный шелкопряд активно продвигается в северном направлении, с средней скоростью 50 км/в год, то в Северо-Западном регионе России этого не происходит и вид распространен намного южнее чем в Западной Сибири. Мы связываем в первую очередь этот феномен с влиянием сезонного распределения температур при глобальном потеплении. В частности, если прирост среднегодовой температуры более выражен в европейской части России, то прирост температур в вегетационный период в два раза выше на участках резко континентального климата, т.е. в западносибирском регионе. Вероятно, как ответ на увеличение прироста летней теплообеспеченности и происходит смещение границ ареала на север в центральной его части, тогда как европейская часть ареала фактически сохраняет свои границы на прежнем месте.
Рисунок — Заселенность непарным шелкопрядом европейской части России.

С помощью дистанционного зондирования земли (ДЗЗ) разработана методика использования индикаторов повреждений непарным шелкопрядом Lymantria dispar L. (Kovalev et al., 2023), где повреждённые участки сравнивались с неповрежденными. В 2024 г. этот подход был модифицирован без необходимости сравнения с неповрежденными. В качестве индикатора повреждения использовали изменения нормализованного разностного индекса растительности (NDVI) в течение сезона. NDVI был использован для выявления дефолиации лесов в Республике Алтай. Результаты показывают, что NDVI на двух дефолированных участках снижался в течение сезона. Пространственное распределение (разрешение 100 м) дефолиации с использованием NDVI показало тенденцию к снижению с 2017 по 2021 год (рис. 1). Более детально метод изложен статье Mori et al., 2024.
Аханаев Ю.Б. (89963817156, akhanaev@mail.ru), Мартемьянов В.В. (89138954756, martemyanov79@yahoo.com)
Публикация: Monitoring and prediction of the spongy moth (Lymantria dispar) outbreaks in Mountain’s landscape using a combination of Sentinel-2 images and nonlinear time series model. Forest ecology and management 2024, 563, 121975 DOI https://doi.org/10.1016/j.foreco.2024.121975. IF 4.33

Протестирован найденный нами ранее новый штамм вируса цитоплазматического полиэдроза (ВЦП) сибирского шелкопряда на разных видах сельскохозяйственно-значимых чешуекрылых с добавлением адьюванта для усиления вирулентности. В результате заражения ВЦП и ВЦП + 0.5% отбеливателем (поверхностно активное вещество усиливающее инсектицидный эффект) приводили к существенному снижению выживаемости гусениц лугового мотылька. Динамика выживаемости гусениц лугового мотылька значительно отличалась от контроля как после заражения ВЦП (х2 = 12.10, df = 5, p = 0.03, рис. 1а), так и после совместного заражения ВЦП с 0.5% отбеливателем (х2 = 70.40, df = 6, p < 0.001, рис. 1б). Выживаемость гусениц в контроле существенно не отличалась от варианта при применении только 0.5% отбеливателя (p = 0.741, рис. 1б). Несмотря на существенное снижение выживаемости гусениц после заражения, дозазависимые эффекты в смертности насекомых не выявлены (рис. 1а,б), из-за чего рассчитать 50% теоретическую летальную концентрацию гибели особей на полученных данных не представляется возможным. Добавление 0.5% отбеливателя в суспензию не повлияло на биологическую активность вируса. Различий в динамике смертности гусениц лугового мотылька после заражения между ВЦП и ВЦП с 0.5% отбеливателем не выявлено (х2 = 0.70, df = 1, p = 0.400). Столь выраженное колебание смертности, не сопряженное с дозой может объяснять отсутствие значимых отличий при анализе восприимчивости гусениц мотылька к циповирусу в нашем предыдущем тестировании (Martemyanov et al., 2023). Не совсем понятно с чем связана такая дисперсия по восприимчивости данного вида, однако в первом приближении, маловероятно, что гусениц лугового мотылька можно рассматривать как целевой объект для инсектицидной обработки с помощью данного вируса. Тем не менее, более детальное исследование может пролить свет на причины столь неустойчивого воздействия вируса. Заражение вирусом гусениц капустной совки не приводило к смертности насекомых (х2 = 4.30, df = 5, p = 0.328) при тестировании линейки доз. Аналогичный результат мы наблюдали на гусеницах капустной совки при заражении ВЦП с 0.5% отбеливателем (p > 0.05).
Таким образом, серия биотестов показала восприимчивость гусениц 2-го возраста лугового мотылька к ВЦП сибирского шелкопряда. При добавлении 0.5% отбеливателя в суспензию вируса наблюдался аддитивный эффект в смертности гусениц. Заражение вирусом гусениц капустной совки не приводило к смертности насекомых, как и при заражении ВЦП с 0.5% отбеливателем. В целом результаты показывают, что синергистические эффекты при использовании ВЦП совместно с 0.5% отбеливателем могут проявляться для некоторых видов насекомых (Martemyanov et. al., 2023) и не проявляться у других. К сожалению, тестирование отбеливателя отечественного производства в схожих концентрациях (0,5%) не выявило увеличение смертности при совместном тестировании с вирусом ВЦП на гусеницах табачного бражника.
Тестирование штамма вируса ВЦП на гусеницах соснового коконопряда показала 80% эффективность вируса при тестировании на гусеницах старших возрастов. К сожалению, ввиду полиморфизма по развитию гусениц и в целом плохой выживаемости, выборка получилась крайне малой, а выживаемость гусениц младших возрастов оказалась низкой. Рассматриваем возможность повторения эксперимента. В случае, если нам удастся найти соснового коконопряда (редкий вид для нашего региона), мы повторим данное исследование на большей выборке. Тем не менее, наличие близкородственного и эффективного вируса у гусениц D. Punctatus (представитель того же рода что и сосновый коконопряд и сибирский шелкопряд) свидетельствует о достаточно высокой степени вероятности воспроизводства полученного результата.
Рис 1а,б. Динамика гибели гусениц лугового мотылька после заражения а) вирусом цитоплазматического полиэдроза сибирского шелкопряда (ВЦП) и б) ВЦП совместно с 0.5% отбеливателем.
Аханаев Ю.Б., Павлушин С.В., Харламова Д.Д. РНФ 23-66-10015
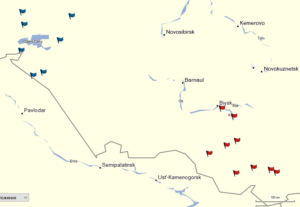
Мониторинг численности непарного шелкопряда проводился в Новосибирской области (НСО) и в Республике Алтай. Для этих целей были установлены феромонные ловушки в регионах и посчитаны количество кладок непарного шелкопряда в НСО.
Во всех ловушках были обнаружены самцы. Численность самцов была намного выше в НСО. Среднее число самцов, отловленных на ловушку, равнялось 450.00±123.50 особей по НСО, на Алтае эта цифра равняется 163.60±30.75 самцов. За 2019-20 гг в открытых источниках (СМИ, информация с РЦЗЛ и т.е.) встречается информация о высокой численности непарного шелкопряда на территории Республики Алтая. Вероятно, в период сбора текущего года шелкопряд находился в фазе спада численности. Места проведения сбора непарного шелкопряда выбраны не случайно. Популяции непарного шелкопряда из НСО и Республики отличаются по поведению. На территории республики самки активно летают и откладывают яйца на отвесных скалах и камнях, что говорит о принадлежности к подвиду Lymantria dispar asiatica. Отловленные самцы были сохранены. Дополнительно были проведены сборы самок в республике. В дальнейшем планируется сравнить крылья между особями из НСО и республики, а также с особями, выращиваемых в лабораторных условиях при питании разными кормовыми растениями.
Учет численности яйцекладок непарного шелкопряда в НСО проводился следующим образом. В период вредоносной деятельности гусениц старшего возраста нами были зафиксированы точки сильной дефолиацией ввиду высокой степени повреждения крон деревьев. Осенью текущего года мы проводили учет яйцекладок непарного шелкопряда в зафиксированных точках. Параллельно, нами были выбраны контрольные точки вблизи очагов, где не наблюдали повреждения кронов, в которых также проводился учет. Учет в каждой точке проводился по двум трансектам вдоль деревьев. Пользуясь этими данными можно проанализировать алгоритм пространственного распределения кладок самками в зависимости от их плотности. Возможны различные варианты реализации групповой стратегии размещения кладок. В настоящей работе проверена оптимизационная модель размещения, минимизирующая риск гибели насекомых в ходе их развития. В результате кладки непарного шелкопряда мы обнаруживали как в очагах, так и в контрольных точках. В очагах количество кладок на дерево было достоверно выше (x2 = 30.09, df = 1, p < 0.001). Так, среднее число в очагах равнялось 8.37±0.25 кладок на дерево, в контроле - 6.65±0.20 кладок. Предположим, что имаго непарного шелкопряда выбирает места для откладки яиц так, чтобы минимизировать некоторую функцию риска гибели гусениц будущего поколения F. Данная функция может зависеть от большего числа неизвестных параметров и найти минимум этой функции не простая задача. Для расчетов функции риска введем в качестве макроскопического параметра, описывающего распределение, величину параметра порядка – долю q деревьев в насаждении, на которых не было найдено кладок. Предположим, что функция F зависит от q и должно выполняться условие, что F(q) стремится к минимуму. Функция F(q) неизвестна, но при q меньшей 1 эту функцию можно разложить в ряд Тейлора, ограничиваясь членом четвертого порядка. Из уравнений (дополнительный материал к отчету) видно, что до некоторого критического значения среднего числа кладок на дереве связь q2 и Х будет характеризоваться линейным уравнением и с увеличением Х доля деревьев без кладок будет падать, а после достижения в насаждении критического числа кладок Хr q =0 и кладки будут встречаться на всех деревьях. Модель можно характеризовать как экологический аналог фазового перехода второго рода в физических системах (Ландау, Лифшиц, 1964; Суховольский и др., 2008). Величина Xr характеризует критическое число кладок на дереве, по достижению которого свободных от кладок деревьев на трансектах не встречается. Параметры уравнения можно найти по данным учетов, где для каждого насаждения вычислялось среднее число кладок на дереве и параметр порядка – долю деревьев без кладок. В этом случае каждое i – ое насаждение будет характеризоваться парой значений (Х(i), q(i)) и можно оценить характер распределения кладок на деревьях для насаждений разных типов, например, для насаждений, в которых реализовалась вспышка массового размножения непарного шелкопряда, и неповрежденных насаждений. Трансекты будем характеризовать как находящиеся в одной из двух фаз: в фазе 1, когда среднее число кладок на дереве на трансекте меньше критического значения Xr для данного года, и в фазе 2, когда среднее число кладок на дереве больше критического значения Xr для данного года. В таблице 1 представлены результаты параметров уравнений в точках учета численности яйцекладок непарного шелкопряда за 2022 г. Параметры А и В, а также критические числа кладок Xr в насаждениях статистически значимо не отличаются, то есть стратегия размещения кладок в насаждениях одинакова. Эти данные можно связать с характеристиками плотности популяции вредителя. При высокой плотности в годы вспышки восприимчивость модели растет, а критическое число кладок падает. Стратегия размещения кладок на деревьях в насаждении носит групповой характер, и по доле q деревьев без кладок и критическому числу кладок можно оценить (хотя бы полуколичественно) плотность популяции вредителя.
Рис 2. Точки расположения феромонных ловушек. Флажки синим цветом обозанчены ловушки на территории НСО, красным – в Республике Алтай
Основные авторы – Ковалев А.В., Аханаев Ю.Б. Работа выполняется при поддержке базового проекта FWGS – 2022 – 0003 и частично РНФ 21-46-07005.

Внешность обманчива: вирусные заболевания, которые даже опытный специалист может воспринять как типичную моноинфекцию, на самом деле могут представлять собой смесь патогенов. Мы обнаружили, что гусеницы непарного шелкопряда, погибшие, на первый взгляд, от типичного полиэдроза (распространенная бакуловирусная инфекция насекомых), содержали в себе целую смесь ДНК и РНК вирусов, включая новый, неизученный ранее вид Hubei lepidoptera virus 3. Смешанные вирусные инфекции могут встречаться гораздо чаще, чем предполагалось. А то, что ранее ошибочно, из-за внешнего сходства, считалось одним видом, может содержать целый комплекс патогенов.
Описание эксперимента по открытию нового вида внутри спонтанной вирусной инфекции
Публикации: Pavlushin SV, Ilinsky YY, Belousova IA, Bayborodin SI, Lunev EA, Kechin AA, Khrapov EA, Filipenko ML, Toshchakov SV, Martemyanov VV. Appearances are deceptive: Three RNA viruses co-infected with the nucleopolyhedrovirus in host Lymantria dispar. Virus Res. (Q2) 2021 May;297:198371. doi: 10.1016/j.virusres.2021.198371. Epub 2021 Mar 5. PMID: 33684420.
Авторы: Павлушин С.В., Белоусова И.А., Аханаев Ю.Б., Мартемьянов В.В.
РНФ № 23-66-10015 (Междисциплинарный проект): «Умный контроль численности чешуекрылых филлофагов-вредителей», 2023-2026гг, 90 млн. руб., Руководитель Мартемьянов В.В.
Эколого-физиологические механизмы поддержания организменного и популяционного гомеостаза в условиях растущего воздействия на экосистемы климатических и антропогенных факторов, Е.А. Новиков, FWGS-2026-0009
Совместные проекты с участием сотрудников лаборатории:
Мегагрант университета Сириус: «Молекулярные подходы в защите растений от насекомых-вредителей как фундамент экологически безопасного природопользования» (2024-2026), 75 млн руб., рук. Павлушин С.В.
FWGS-2021-0003, Гомеостаз популяций и сообществ: адаптации животных к меняющимся условиям среды, рук. Е.А. Новиков
РФФИ 19-416-543005 р_мол_а "Новый подход в использовании адъювантов для совершенствования биопрепаратов против насекомых-филлофагов на основе миксинфекции" (2019-2020). 1,2 млн. руб. Руководитель Аханаев Ю.Б.
РФФИ № 19-416-540005 «Изучение смешанных инфекций непарного шелкопряда и моделирование их динамики в различных погодных и климатических условиях как основа для разработки комбинированного биологического продукта» (2019-2020). 1,5 млн руб. Рук. Мартемьянов В.В.
РФФИ № 15-04-08197-а. Взаимосвязь между состоянием защитных систем непарного шелкопряда и переходом бакуловирусной инфекции из скрытой формы в острую. (2015-2017). 2.1 млн. рублей. Руководитель Павлушин С.В.
РФФИ № 15-29-02676-ОФИ. Законы регулирования численности популяций непарного шелкопряда в лесных экосистемах: от молекулярных механизмов до управления популяциями. (2015-2017). 3 млн. руб. Руководитель Мартемьянов В.В.
РФФИ № 18-34-20060 мол_а_вед: "Влияние кишечной микробиоты насекомых на развитие патогенезов, вызываемых энтомопатогенными грибами и бактериями", (2018-2019), Руководитель Ярославцева О.Н.
РНФ № 21-46-07005 (Международный проект Россия-Япония): «Усовершенствованная интегрированная система управления популяций лесных вредителей основанная на их удаленном мониторинге», 2021-2023, 42 млн. руб., руководитель Мартемьянов В.В.
РНФ № 20-64-46011 (Проект ведущие ученые с международным участием): «Оценка адаптационных возможностей двух основных видов денрофильных филлофагов умеренных широт при их экспансии на север в связи с глобальным изменением климата», 2020-2022, 24 млн. руб., Руководитель Мартемьянов В.В.
РНФ № 17-46-07002 (Международный проект Россия-Япония): «Изучение жизненных стратегий вируса ядерного полиэдроза непарного шелкопряда в различных климатических условиях для эффективного управления популяциями дендрофильных филлофоагов», 2017-2019, 42 млн. руб., Руководитель Мартемьянов В.В.
РНФ № 21-46-07005 (Молодежный): «Механизм вертикальной передачи бакуловирусной инфекции», 2021-2022, 3 млн руб., Руководитель Белоусова И.А.
РНФ № 17-76-10029 (Молодежный): «Полоспецифичность в формировании резистентности чешуекрылых – новая фундаментальная основа для эффективной регуляции численности насекомых» (2017-2020), 3 млн руб. Руководитель Павлушин С.В.
РНФ № 23-16-00262: «Методы, технологии и системы массового размножения чешуекрылых насекомых как основа производства энтомопатогенов и энтомофагов, применяемых в борьбе с сельскохозяйственными и лесными вредителями», (2023-2025), 21 млн. руб., Руководитель Токарев Ю.С.
РНФ № 20-66-46009: «Взаимоотношения микроспоридий с другими эндоцитобионтами и энтомофагами чешуекрылых насекомых на организменном и популяционном уровне» (2020-2022), 21 млн. руб., Руководитель Токарев Ю.С.
РНФ № 15-14-10014 (с участием постдоков): «Механизмы резистентности насекомых к энтомопатогенным микроорганизмам и разработка новых подходов для развития биологических методов контроля численности насекомых - вредителей сельского и лесного хозяйства» (2015-2017), 24 млн. руб., Руководитель Глупов В.В.
Блок текста
Блок текста
Блок текста