
Исследование филогенетики и филогеографии различных групп гидробионтов Евразии и особенности их экологии.
Адаптивные механизмы функционирования пищеварительной системы морских и пресноводных видов рыб, в том числе важных для отечественной аквакультуры.

В результате исследования сообществ паразитов рыб Байкальской рифтовой зоны получены новые сведения о видовом разнообразии цестод рыб оз. Байкал. На основании филогенетического анализа последовательностей генов 28S и cox1 показано, что цестоды рода Proteocepalus от Coregonus migratorius из оз. Байкал образуют отдельную кладу видового уровня с высокой поддержкой (Рисунок 1). При этом у сигов Цыпо-Ципиканской системы озер (Республика Бурятия) также зарегистрирован вид рода Proteocephalus, который не был отмечен за пределами этой озерной системы. В кишечнике обыкновенного сига из озера Цагааннур (Монголия), расположенном в Дархатской котловине на юге Байкальской рифтовой зоны отмечен третий вид цестод рода Proteocephalus, который также был зарегистрирован у C. lavaretus в Телецком озере (Республика Алтай) и у C. muksun в устье реки Яна (Якутия). Таким образом, у рыб рода Coregonus в озерах Байкальской рифтовой зоны отмечены три вида Proteocephalus spp., два из которых нигде более не отмечены.
Рисунок. Филогенетические деревья, рассчитанные для последовательнотей 28S и cox1 от цестод из Coregonus spp.
Основные авторы: Власенко П.Г., Колмогорова Т.В.
Источник финансирования: базовый проект, РНФ 23-74-10101
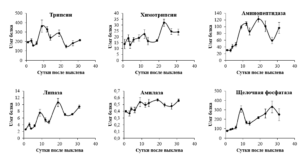
Активности ключевых групп пищеварительных ферментов, отвечающих за полостное (пепсин, трипсин, химотрипсин, липаза и амилаза) и пристеночное (щелочная фосфатаза и аминопептидаза) пищеварение были проанализированы начиная с первого до 31-го дня после выклева личинок из икры. Нельма выращивалась в пластиковых бассейнах по стандартной методике. Активность всех пищеварительных ферментов определялась спектрофотометрически с применением соответствующих субстратов и специфических условий реакций. В результате проведенной работы было выявлено два-три пика активности между 9 и 12, а также 19 и 27 сутками после выклева. Для всех ферментов (за исключением трипсина) наблюдалось постепенное увеличение активности с момента выклева до 19 – 27-х суток. Активность основной протеазы желудка – пепсина не детектировалась до 14 суток после выклева, после чего наблюдалось резкое увеличение активности до 27-х суток с последующей стабилизацией. Полученные результаты позволят скорректировать состав искусственных кормов для лучшего их соответствия паттернам изменения специфической активности пищеварительных ферментов, что должно положительно сказаться на скорости роста и выживаемости нельмы в раннем онтогенезе.
Рисунок. Онтогенетические измененния активности панкреатических и пристеночных пищеварительных ферментов нельмы.

Получены 55 последовательностей 28S длинной 1540 нуклеотидов и 32 последовательности cox1 длиной 1548 нуклеотидов. В результате филогенетического анализа последовательности 28S от цестод из кишечников лососевых рыб были включены в большую слаборазрешенную кладу вместе с P. percae, внутри которой клады с высокой (>75%) бутстрэп-поддержкой образовали последовательности от сигов из оз. Баунт и часть последовательностей от гольцов с Кроноцкого озера. В результате анализа по cox1 последовательности от цестод из кишечников сигов озер Телецкое и Цагааннур, сигов из Верхнего Ондомозера, сигов из Баунта образовали клады видового уровня с высокой (100%) бутстрэп-поддержкой. Также две отдельные клады с максимальными значениями поддержки были образованы последовательностями от цестод из гольцов Кроноцкого озера. В одну из этих клад вошла последовательность цестоды из оз. Гытгыл (рис.). На основании анализа молекулярных данных мы предполагает наличие у сигов в Евразии минимум трех видов цестод, у гольцов минимум двух видов цестод рода Proteocephalus. Такой результат показывает ошибочность представления о голарктическом распространении P. longicollis.
Филогенетическое дерево последовательностей гена cox1 Proteocephalus spp., построенное методом присоединения соседей. Место сбора материала и хозяева показаны для клад, образованных оригинальными последовательностями. Цветом выделены клады цестод от лососевых рыб.
авторы: Власенко П.Г., Кашинская Е.Н., Соловьев М.М.
Финансирование: РНФ 23-74-10101
Сиги Coregonus lavaretus s. l. в Сибири представлены множеством экологически и морфологически дистантных форм. Часть из них генетически обособлена, другие имеют неопределенный статус (однообразные пыжьяновидные сиги из арктических частей крупных рек). Формы дифференцируют по экологии: планктофаги/бентофаги, речные, озерно-речные, озерные. Считается, что они хорошо различаются морфологически: внимание обращают на размер головы, высоту тела, длину и высоту хвостового стебля. Согласно правилу, речные рыбы имеют более высокий и короткий хвостовой стебель и вальковатое тело, озерные — более высокое и уплощенное. Однако для сигов это правило, похоже, не работает.
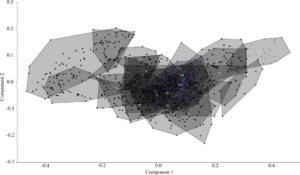
Наш анализ изменчивости пыжьяновидных сигов показал, что постулируемые различия между озерными и речными формами не всегда подтверждаются. Метод главных компонент: в первую главную компоненту (55,14 %) наибольший вклад дали признаки формы тела, признаки головы — отрицательный. Вторую компоненту (10,50 %) не рассматривали.
Рис. Распределение выборок сигов из водоемов Сибири в пространстве двух первых главных компонент по пластическим признакам. 1-сиг телецкий, 2-сиг Правдина, 3-сиг ох. Каракуль, 4-сиг р. Абакан, 5-сиг оз. Тоджа (озерный), 6-сиг оз. Тоджа (речной), 7-C. baunti (оз. Капылюши), 8-озерно-речной сиг оз. Капылюши, 9-ряпушковидный сиг оз. Баунт, 10-озерно-речной сиг оз. Доронг, 11-озено-речной сиг оз. Баунт, 12-среднетычинковый сиг оз. Доронг, 13-среднетычинковый сиг оз. Баунт, 14-речной сиг р. Анабар, 15-озерный (лиманный) сиг р. Анабар, 16-речной сиг р. Кутарамакан, 17-озерный сиг оз. Кутарамакан, 18-озерный (лиманный) сиг Быковская протока р. Лена, 19-речной сиг р. Лена (устье р. Буотама), 20- озерный (лиманный) сиг р. Яна, 21- речной сиг р. Витим, 22-озерный сиг (C. jucagiricus) оз. Илирней.
Среднепопуляционные величины сортировали по максимальной высоте тела. Наименьшая высота тела и хвостового стебля, наибольшая его длина — у среднетычинковых озерных планктофагов Южной Сибири. Южно-сибирские речные сиги максимально высокотелы с коротким и высоким хвостовым стеблем. Арктические речные — низкотелы с низким хвостовым стеблем. Озерные арктические — более высокотелы с короткой головой.
Кластерный анализ (UPGMA) дал два кластера. В первый вошли сиги-планктофаги Южной Сибири (Баунтовские озера, Телецкое) — с наименьшей высотой тела, длинным и низким хвостовым стеблем. Второй включает три субклады: 1) высокотелые озерные арктические сиги (Анабар, Кутарамакан, Быковская протока Лены и Яны, оз. Илирней); 2) озерные низкотелые и речные высокотелые сиги Южной Сибири, а также речные низкотелые арктические; 3) низкотелые озерные сиги Южной Сибири и низкотелый речной сиг из Лены.
Речные пыжьяновидные сиги Сибири генетически неоднородны. Арктические речные соответствуют описанию Никольского (низкое тело, низкий и длинный хвостовой стебель), южно-сибирские речные — максимально высокотелы с коротким и высоким хвостовым стеблем. Эти противоречия указывают на существование немногих древних филогенетических линий, сформировавших современное разнообразие форм/видов.
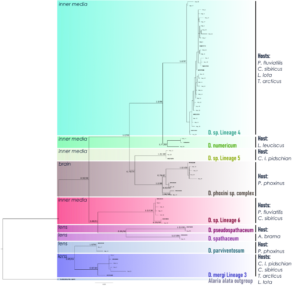
В результате изучения видового состава трематод р. Diplostomum озеро Телецкое было осмотрено 8 видов рыб. Для оценки уровня зараженности озера и сбора метацеркарий Diplostomum в общей сложности наблюдали 449 особей: гольян Phoxinus phoxinus (n=12), елец Leuciscus leuciscus (n=11), лещ Abramis brama (n=3), налим Lota lota (n=39), окунь Perca fluviatilis (n=66), сибирский подкаменщик Cottus sibiricus (n=38), сиг Телецкий Coregonus lavaretus pidschian (n=135), сиг Правдина C. lavaretus pravdinellus (n=65), хариус Thymallus arcticus (n=41), щука Esox lucius (n=33). По экологическим показателям зараженности общий уровень зараженности составил 38,82%, а общая среднее обилие – 18,027 (1-298) В результате секвенирования фрагмента гена cox1 паразитов, полученных из Телецкого озера, были получены 74 новые последовательности, объединенные в 52 гаплотипа и проанализированные вместе с 49 последовательностями филогенетических линий видового уровня Diplostomum, извлеченными из базы данных NCBI GenBank на основе последних данных по таксономии Diplostomum. В результате Bayesian Inference и Maximum Likelihood анализа топологии деревьев оказались согласованными. Все полученные последовательности кластеризовались в 11 взаимно монофилетических высокоподдерживаемых клад: D. sp. Lineage 5 и D. sp. Lineage 6, D. petromyzifluviatilis, D. numericum, D. spathaceum, D. pseudospathaceum, 'D. phoxini Lineage 1', 'D. phoxini Lineage 2', 'D. phoxini Lineage 3' и 'D. mergi Lineage 3' с наибольшей межвидовой дивергенцией (нескорректированные p-дистанции) 16,22%. Все клады "не-хрусталиковых" видов и клады "хрусталиковых" видов имеют тенденцию группироваться близко друг к другу и имеют между собой меньшую генетическую дистанцию.
Основные авторы: Власенко П.Г., Изотова Г.В., Соловьев М.М.
РНФ 19-74-10054П, Мега-грант 075-15-2022-1134
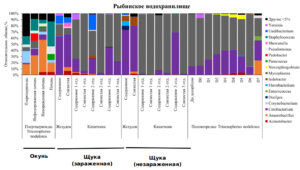
Кишечная микробиота щуки Esox lucius. По результатам секвенирования V3-V4 региона гена 16S рРНК наибольшее количество вариантов последовательностей ампликонов (amplicon sequence variant, ASV) и разнообразие бактерий по индексу Шеннона отмечено для ассоциированной микробиоты слизистой и содержимого желудка незараженных щук (ASV: 22.8±6.5 и 37.0±15.5, Шеннон: 1.0±0.2 и 1.5±0.4, соответственно), наименьшее – для слизистой кишечника незараженной щуки (ASV: 9.8±3.4, Шеннон: 0.5±0.2). Достоверных отличий по количеству ASV и индексу Шеннона между кишечной микробиотой зараженных и незараженных щук не выявлено (тест Данна, p>0.05). В составе микробиоты слизистой и содержимого желудка зараженной и незараженной щуки из Рыбинского водохранилища доминировали Mycoplasma и Cetobacterium. В качестве субдоминантов в желудке зараженной щуки отмечены Undibacterium, Shewanella и Yersinia, а в желудке незараженных рыб, - Flavobacterium и Iodobacter. В микробиоте различных отделов кишечника зараженных и незараженных рыб отмечен сходный состав доминантов, с высоким обилием выявлены Acinetobacter, Anaerorobacillus, Mycoplasma и Cetobacterium (рис.).
Микробиота половозрелых цестод T. nodulosus, паразитирующих в кишечнике щуки. Число ASV в смывах бактерий с тегумента цестод достоверно не отличалось между собой (тест Данна, p>0.05) и варьировалось в пределах 8.3±2.1 – 13.8±2.4. Значения индекса Шеннона, напротив, достоверно отличались при сравнении смывов D7 со смывами D1, D2 и D7 (тест Данна, p≤0.05). В ассоциированной микробиоте половозрелых цестод T. nodulosus, паразитирующих в кишечнике щуки, доминировали Mycoplasma и Cetobacterium, причем относительное обилие Cetobacterium в ряду смывов D0-D4 увеличивалось, а обилие Mycoplasma – снижалось. Начиная со смыва D3 и заканчивая D5 в микробиоте цестод появляются Acinetobacter, Novosphingobium и Flavobacterium. В микробиоте D6 снова доминируют только Mycoplasma и Cetobacterium. Во фракции D7 (черви после всех смывов) доминировали Anaerorobacillus, Cetobacterium и Enteroccous.
Микробиота плероцеркоидов T. nodulosus, паразитирующих в печени окуня. Число ASV и разнообразие по индексу Шеннона в микробиоте плероцеркоидов T. nodulosus и микробиоте печени достоверно не отличалось между собой и варьировало от 8.9 до 21.8 и 1.8 до 2.8, соответственно. Ассоциированная микробиота плероцеркоидов T. nodulosus, паразитирующих в печени окуня, существенно отличалась от состава бактерий, выявленных у половозрелых цестод из кишечника щуки. Так в микробиоте плероцекоидов T. nodulosus доминировали Anaerobacillus, Corynebacterium и Staphylococcus. В печени зараженных окуней в большом количестве выявлены Anaerobacillus, в печени неараженных рыб, напротив, доминировали Staphylococcus. Бактерии рр. Cetobacterium и Pedobacter выявлены только в печени зараженных рыб, а Paracoccus отмечен в печени только у незараженных рыб (рис. 9.1).
Рисунок 9.1. Относительное обилие бактерий на уровне рЫода в микробиоте плероцеркоидов T. nodulosus, паразитирующих в печени окуня, и половозрелых T. nodulosus из кишечника щуки из Рыбинского водохранилища.
Основные исполнители: Власенко П.Г., н.с., Кашинская Е.Н., с.н.с., к.б.н. Хоменко Ю.С., м.н.с., Симонов Е.П., с.н.с., к.б.н., Соловьев М.М., в.н.с., к.б.н. Тематическая группа физиологии и генетики гидробионтов.
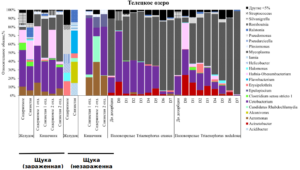
Кишечная микробиота щуки Esox Lucius. Наибольшее количество ASV и разнообразие бактерий по индексу Шеннона отмечено для ассоциированной микробиоты содержимого желудка зараженных щук (ASV: 34.5±6.2, Шеннон: 1.6±0.3), наименьшее – для слизистой первого отдела кишечника зараженной щуки (ASV: 15.5±1.5, Шеннон: 1.4±0.1). Микробиота слизистой и содержимого желудка зараженных щук характеризовалась сходным составом доминантов. В составе микробиоты слизистой и содержимого желудка зараженной щуки из оз. Телецкое доминировали Aeromonas, Cetobacterium, Clostridium sensu stricto1, Hafnia-Obesumbacterium и Silvanigrella. В то же время для незараженных рыб состав доминантов в слизистой и содержимого желудка существенно отличался. Так, в содержимом желудка отмечены Halomonas, Helicobacter, Pseudarciella, Pseudomonas и Streptococcus, в слизистой доминировали Alcanivorax, Erysipelothrix, Flavobacterium и Ralstonia. В содержимом различных отделов кишечника зараженных щук преобладали Cetobacterium и Hafnia-Obesumbacterium, в слизистой доминировали Cetobacterium и Mycoplasma. У незараженных рыб по сравнению с зараженными в содержимом кишечника доминировали Aeromonas, Candidatus Rhabdochlamydia и Epulopiscium, слизистая кишечника в основном представлена бактериями рр. Aeromonas и Cetobacterium (рис. ).
Микробиота половозрелых цестод T. nodulosus и T. crassus, паразитирующих в кишечнике щуки. Число ASV и разнообразие бактерий по индексу Шеннона в ассоциированной микробиоте цестод T. nodulosus было выше по сравнению с T. crassus, однако достоверных отличий по тесту Данна не наблюдалось (p>0.05). В Телецком озере в ассоциированной микробиоте половозрелых цестод T. nodulosus и T. сrassus, паразитирующих в кишечнике щуки, также доминировали Mycoplasma и Cetobacterium. Относительное обилие Cetobacterium в ряду смывов D0-D7 снижалось, а Mycoplasma, наоборот, увеличивалось. Для ассоциированной микробиоты T. nodulosus и T. сrassus также с высоким обилием отмечены Acinetobacter и Hafnia-Obesumbacterium, доля которых также снижалась в ряду смывов D0-D7.
Микробиота плероцеркоидов T. nodulosus и T. crassus, паразитирующих в печени и мышцах различных промежуточных хозяев. В микробиоте плероцеркоидов, паразитирующих в мышцах и печени вторых промежуточных хозяев (сиг Правдина, телецкий сиг, сибирский подкаменщик, хариус и налим) общими доминирующими таксонами бактерий выступали Acinetobacter, Anaerobacillus и Halomonas. Микробиота плероцеркоидов T. crassus сига Правдина и телецкого сига не отличалась между собой. Основные отличия в ассоциированной микробиоте плероцеркоидов T. nodulosus у различных промежуточных хозяев вносили бактерии рр. Erysipelothrix для сибирского подкаменщика, Serratia для хариуса и Neorickettsia для налима.
Таким образом, в результате проведенных исследований впервые охарактеризована микробиота, ассоциированная с цестодами из р. Triaenophorus на разных стадиях развития (плероцеркоиды и половозрелые черви) и их промежуточных и дефинитивных хозяев из разнотипных водоемов России (олиготрофное Телецкое озеро и эвтрофное Рыбинское водохранилище). Микробиота цестод рода Triaenophorus на разных стадиях жизненного цикла (плероцеркоиды и половозрелые черви) характеризовалась различным составом бактериальных сообществ. Различия в составе бактерий, ассоциированных с цестодами рода Triaenophorus, прослеживались не только от стадии их жизненного цикла, но и от вида промежуточного хозяина и типа водоема. Среди общих доминантов, встречающихся в составе микробиоты половозрелых червей, выявлены Mycoplasma и Cetobacterium, а в микробиоте плероцеркоидов – Acinetobacter, Anaerobacillus и Staphylococcus. По результатам проведенных исследований показано, что микробиота, ассоциированная с плероцеркоидами цестод, достоверно не отличалась от микробиоты их капсул и мышц/печени, из которых были извлечены эти паразиты. В тоже время микробиота, ассоциированная с половозрелыми цестодами рода Triaenophorus из кишечника щуки, достоверно отличалась от микробиоты плероцеркоидов.
Рисунок. Относительное обилие бактерий на уровне рода в микробиоте половозрелых T. crassus и T. nodulosus из кишечника щуки из Телецкого озера.
Основные исполнители: Власенко П.Г., н.с., Кашинская Е.Н., с.н.с., к.б.н. Хоменко Ю.С., м.н.с., Симонов Е.П., с.н.с., к.б.н., Соловьев М.М., в.н.с., к.б.н. Тематическая группа физиологии и генетики гидробионтов.

Были исследованы метацеркарии от десяти видов рыб: сазана, серебряного и золотого карася, плотвы, ельца, язя, леща, окуня, судака и щуки. Всего получено 74 нуклеотидных последовательностей cox1 и 20 последовательностей кластера ITS1–5.8S-ITS2 длиной 595 и 949-1065 нуклеотидов соответственно. В результате филогенетического анализа все последовательности cox1 образовали 3 клады видового уровня с высокой поддержкой. Две из них, с локализацией метацеркарий в хрусталиках рыбы, были определены как D. spathaceum и D. pseudospathaceum. Третья клада сформирована последовательностями от метацеркарий из внутренней среды глаза была определена как D. volvens.
Всего от метацеркарий из глаз рыб оз. Чаны для фрагмента cox1 длиной 587 нуклеотидов отмечено 18 гаплотипов для D. spathaceum (Hd = 0,977±0,016, Pi = 0,008±0,0008), 29 гаплотипов для D. pseudospathaceum (Hd = 0,975±0,011, Pi = 0,0055±0,0005) и 5 гаплотипов для D. volvens (Hd = 0,933±0,122, Pi = 0,0064±0,0017).
pseudospathaceum зарегистрирован в хрусталиках всех исследованных видов рыб. Непосредственно из озера Чаны для этого вида зарегистрировано 29 гаплотипов при Hd = 0,975±0,011и Pi = 0,0055±0,0005. При использовании последовательностей из Генбанка для анализа распространения гаплотипов этого вида использовано выравнивание длиной 450 нуклеотидов. При анализе полученного выравнивания отмечено 32 гаплотипа. На медианной сети гаплотипов отчетливо выделяется центральный гаплотип, который был отмечен из Чанов, Румынии и Германии. Максимальная попарная p-дистанция для D. pseudospathaceumсоставила 0,0177±0,0036 при средней 0,0046 (Длина 453).
spathaceum обнаружен нами в хрусталиках восьми (сазан, серебряный и золотой караси, плотва, елец, язь, окунь, судак) видов. От исследованных нами метацеркарий отмечено 18 гаплотипов при Hd = 0,977±0,016 и Pi = 0,008±0,0008. После привлечения доступных данных из ГенБанка получено итоговое выравнивание длиной 425 нуклеотидов. На основании этого выравнивания отмечено 57 гаплотипов, из которых можно выделить 2, отмечаемые с наибольшей частотой. Эти гаплотипы отмечены из Чанов, Китая, Турции, Ирака и Украины. Также общие с Чанами гаплотипы отмечены из Германии. Наибольшее разнообразие гаплотипов отмечено в Ираке, где проходит зимовка птиц, зараженных маритами Diplostomumspp. Максимальная попарная p-дистанция D. spathaceum0,0189±0,0067 при средней 0,0058 (Длина 430).
volvens. Метацеркарии D. baericomplex sp. 2 обнаружены только во внутренней среде глаза окуня. Близкие к полученным нами последовательности были ранее отнесены к комплексу видов D baeriкак D. baeri Lineage 2’ (Georgieva et al., 2013). Однако Faltýnková et al. (2022) опровергли это определение. Было показано, что эти последовательности принадлежат трематодам, которые хоть и близки к D baeri морфологически, однако реализуют свой жизненный цикл через других вторых промежуточных хозяев и имеют другую локализацию внутри глаза. В целом, обнаруженные нами метацеркарии по своим признакам, таким как виды рыб-хозяев и локализация в глазах рыб, более соответствуют D. volvens в понимании Шигина (1993). В исследованном нами материале отмечено 5 гаплотипов для D baeri при Hd = 0,933±0,122 и Pi = 0,0064±0,0017. При использовании последовательностей из Генбанка для анализа распространения гаплотипов этого вида использовано выравнивание длиной 356 нуклеотидов. Всего для итогового выравнивания отмечено 32 гаплотипа. При анализе мединной сети гаплотипов можно выделить 3 центральных, которые помимо Чанов отмечены в Исландии, Германии, Норвегии и в Северо-Западной России. Максимальная попарная p-дистанция для D. baeri 0,02247±0,0078 (длина 356 п.н.), при средней 0,00856.
Рисунок. Филогенетическое дерево для последовательностей cox1, построенное методом максимального правдоподобия. В качестве аут группы использованы последовательности Tylodelphys clavata.
Основные исполнители: Власенко П.Г., н.с., Кашинская Е.Н., с.н.с., к.б.н. Хоменко Ю.С., м.н.с., Симонов Е.П., с.н.с., к.б.н., Соловьев М.М., в.н.с., к.б.н. Тематическая группа физиологии и генетики гидробионтов.

Основные результаты исследований были направлены на изучение в сравнительном аспекте структурных особенностей ассоциированной микробиоты паразитов рыб в зависимости от устройства их пищеварительной системы, а также микробиоты хозяина в месте локализации исследуемых паразитов.
Впервые охарактеризовано микробное сообщество кишечника и других частей «тела» (кутикула, мышцы) нематод Cystidicola farionis, паразитирующих в плавательном пузыре носатого гольца различных морфологических групп из оз. Кроноцкое, п-ов Камчатка (рис. 1).
В кишечнике и «теле» нематод преобладали бактерии рр. Aeromonas, Pseudomonas, Shewanella и Yersinia. Доминирующая микробиота плавательного пузыря представлена Acinetobacter, Cetobacterium, Pseudomonas, Shewanella, Yersinia и неклассифицированными Enterobacteriaceae. В ассоциированной микробиоте нематод и плавательного пузыря выявлены уникальные таксоны бактерий. Так, бактерии р. Paracoccus были зарегистрированы только в микробиоте, ассоциированной с плавательным пузырем, а бактерии р. Lawsonella, Staphylococcus, Tumebacillus и неклассифицированные Alicyclobacillaceae были обнаружены в микробиоте кишечника и «тела» нематод.
Достоверно наибольшее количество операционных таксонобразующих единиц (ОТЕ) и наибольшие значения индекса Чао1 зарегистрировано в микробиоте кишечника нематод по сравнению с микробиотой, ассоциированной с плавательным пузырем.
Характеристики альфа-разнообразия ассоциированной микробиоты нематод, паразитирующих в плавательном пузыре носатого гольца формы N2 были значительно выше по сравнению с микробным сообществом нематод, паразитирующих у рыб формы N1g.
Рисунок 1. Нематоды Cystidicola farionis (б), паразитирующие в плавательном пузыре носатого гольца Salvelinus malma complex различных экологических групп (а).
Основные исполнители: Кашинская Е.Н., Власенко П.Г., Симонов Е.П., Шокурова А.В., Хоменко Ю.С., Соловьев М.М. Источник финансирования РНФ
2026-2030: Эколого-физиологические механизмы поддержания организменного и популяционного гомеостаза в условиях растущего воздействия на экосистемы климатических и антропогенных факторов (Е.А. Новиков), FWGS-2026-0009
Министерство науки и высшего образования РФ, грант в форме субсидии Федеральной научно-технической программы развития генетических технологий на 2019-2027 годы, Rf-193021X0012, 2021-2023, Лисица А.В.
РНФ 23-74-10101, 2023-2026, Кашинская Е.Н.
РНФ 23-74-10101, 2023-2026, Кашинская Е.Н.
РНФ, 23-74-10101, 2023-2026, Кашинская Е.Н.
2014-2020: 0311-2017-0014: Эколого-физиологические, онтогенетические и поведенческие аспекты жизненных циклов позвоночных животных. Рук. Г.Г. Назарова
2021-2025: FWGS-2021-0003: Гомеостаз популяций и сообществ: адаптации животных к меняющимся условиям среды. Рук. Новиков Е.А
РФФИ, 20-40-00610, 2020-2023, Зуйкова Е.И.
РФФИ, 20-54-44017, 2020-2023, Монг_а, 2020-2023, Суханова Л.В.
РФФИ, 19-04-00964, 2019-2021, Крутовский К.В.
РНФ 19-74-10054, 2022-2024, Соловьев М.М.
РНФ 24-24-00528, 2024-2025, Зуйкова Е.И.
РНФ, 19-14-00218, 2019-2021, Левин Б.А.
РНФ, 19-74-00104, 2019-2021, Кашинская Е.Н.
РНФ, 19-74-10054, 2019-2022, Соловьев М.М.
РНФ, 19-74-10054П, 2022-2024, Соловьев М.М.
РНФ, 21-74-10107, 2021-2024, Симонов Е.П.
Блок текста
Блок текста
Блок текста